受2021年开始的“资本寒冬”影响,全球医药市场迎来周期性“融资寒冬”,寒冬”中的投资人更为审慎——投资项目更少、投资金额更小。资本市场“寒冬”也让创新药企开始审视竞争市场,理性思考自身团队和产品竞争力,展开自救。
TransCode Therapeutics已经到了生存紧要关头。
作为一家拥有七条管线的创新基因药物公司,TransCode Therapeutics的22年底现金储备仅500万美元,股票市值仅223.54万美元。与此同时,TransCode的癌症靶向药物开启了新药首次人体临床试验(FIH)。
身处“寒冬”,现金储备500万美元的创新医药企业如何断臂求生?
TransCode一直在自救。
今年2月14日,TransCode撤回了此前发布的股票发行注册声明,股票迎来大量交易,15日成交量达4000万,盘前交易中股价上涨了100%。17日,TransCode完成每股价值0.527美元的285万股普通股的注册直接发行,净收益130万美元。
4月5日,TransCode获得NIH颁发的SBIR(小企业创新研究快速通道)第三年赠款,这一赠款总额约87.1万美元。4月14日,TransCode完成了白狮资本的股权融资,将于5月31日前向其出售约108万美元普通股。
而另一方面,自救而发行的大量股权让TransCode失去了股价优势。持股人担心股权被稀释、股票价格受新发行定价影响下跌,甚至带来了潜在的退市风险。以2个月为限,TransCode1月至3月单股股票未跌下8美元,3月至5月单股股票从未高于8.7美元,年度波幅高达每股34.65美元。
TransCode显然也意识到了这个问题。5月,TransCode进行了1:20反向股票拆分调整,以提高公司普通股的交易价格,使公司满足纳斯达克的最低出价要求。这一分割自动将20股普通股合成为1股,已发行股票数量将从约1700万股减少到约85万股。
但效果不佳,5月25日以来,股价跌下从未有过的5美元大关。TransCode依旧捉襟见肘。
尽管如此,TransCode依然开启了新一轮公开募股。6月6日,TransCode发行了定价700万美元的公开募股。每股公开发行价格为3.50美元。每股普通股附加3.25美元的行使价格,即可购买一股A-1系列认股权证或A-2系列认股权证。两类认股权证都可立即行使,自签发之日起三年到期。
认股权证的本质上是TransCode在出售自己的未来。
未来在哪里?很显然,TransCode的答案是递送平台与药物管线。
TransCode致力于通过智能设计和有效递送RNA疗法来战胜癌症,其专利产品是一个纳米药物递送平台TTX系统。
TTX输送系统是一种以氧化铁纳米颗粒作为物质载体的RNA传递平台。氧化铁纳米颗粒所具有的超顺磁性质、生物相容性、低毒性、低免疫原性等特性使其可应用于生物医学,目前已被批准作为临床癌症显像剂和缺铁性贫血治疗方案。
在TTX传送系统中,氧化铁纳米颗粒能够减少早期肾脏和肝脏清除,转化为较长的循环半衰期,在肿瘤和转移部位有效积累。另外,其内置成像能力有利于完成定量粒子向靶向器官的输送,且有望实现对于肝脏和肾脏外靶点的递送。
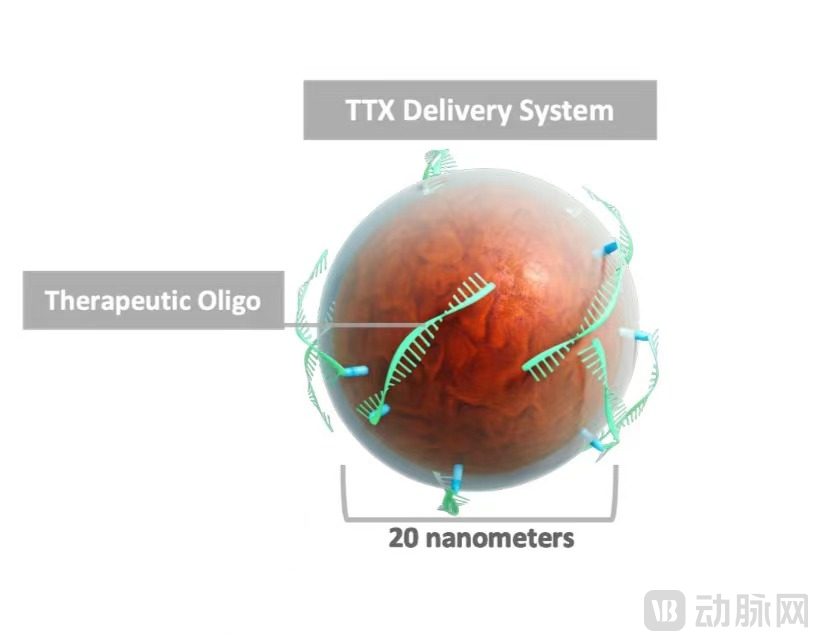
TTX递送系统模型
图片来源:TransCode官网
在进一步制备中,核心氧化铁复合物与葡萄糖聚合物右旋糖交联,为颗粒提供整体稳定性。右旋糖酐涂层和氧化铁芯被氨基功能化,形成稳定的连接,以搭载治疗性寡核苷酸。这一复合物的设计保护了寡核苷酸,使其免受降解。
复合物的小尺寸血流动力学分布和正电荷使它们能够渗透到肿瘤微血管中,外渗至肿瘤间质和转移瘤间质中,易于细胞吸收。同时,右旋糖酐涂层利用癌细胞的高代谢活性,进一步加速了颗粒吸收。血流动力学分布和代谢触发吸收的综合效果增强了TransCode纳米颗粒进入肿瘤细胞内遗传靶点的能力。
相比传统递送方式或有机纳米递送,TTX递送系统具有低风险高效果的优势:
1-对RNA靶点的高结合亲和力和高特异性;
2-低毒性、低免疫原性、已证实的临床安全性;
3-高稳定性,可适应各种类型的有效载荷,可冻干保存,无需冷链运输;
4-利用质子海绵效应实现高效率的细胞输送;
5-可应用于神经学,通过MRI和药物生物利用度测量进行定量非侵入成像检测;
6-高可调性,高灵活性,可根据目标组织进行载体调整。
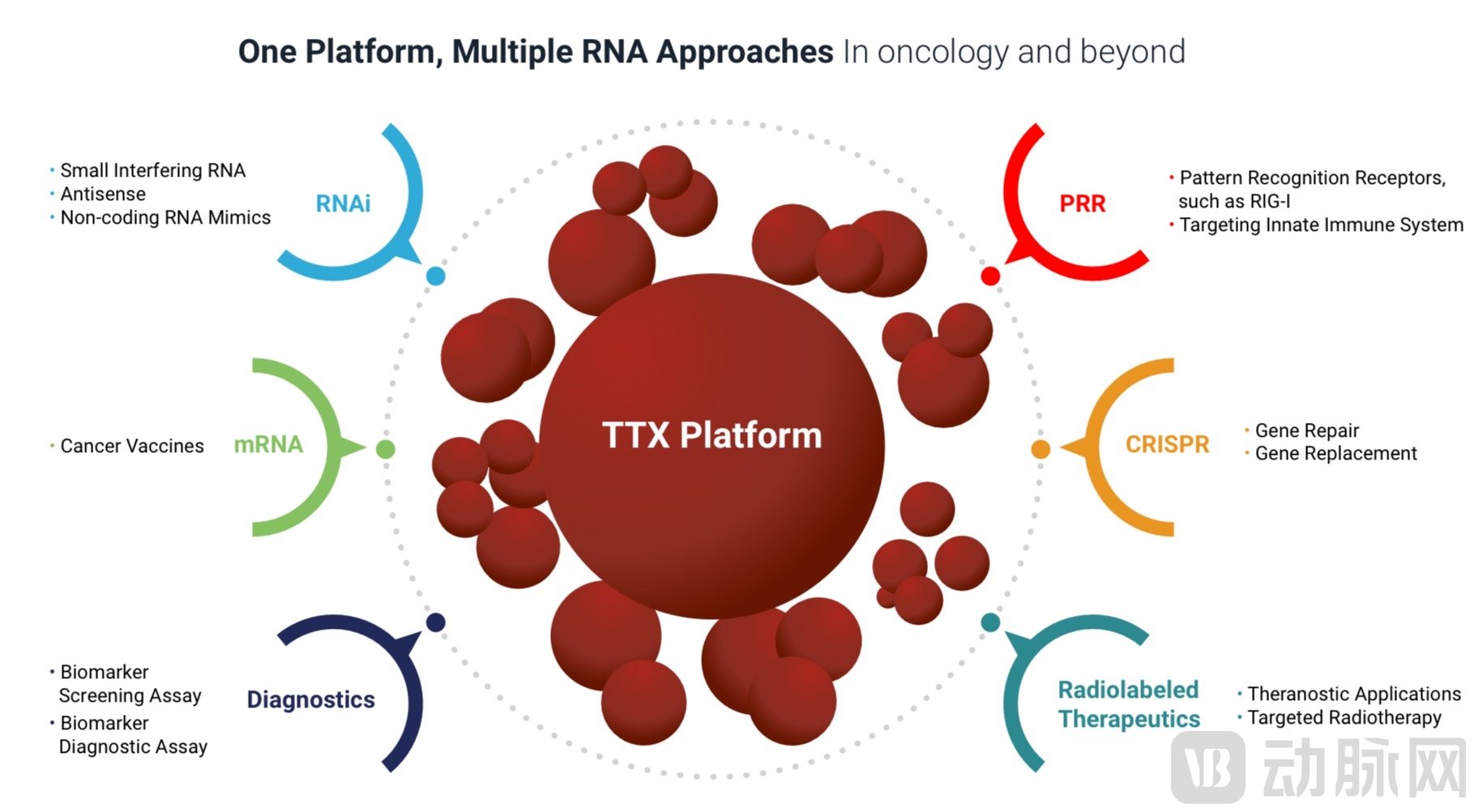
TTX系统候选RNA治疗方案
图片来源:TransCode官网
TTX系统能够适用于多种RNA治疗方案。据此,TransCode搭建了七个不同的候选治疗产品系列,以改善癌症患者和预后和长期生存。
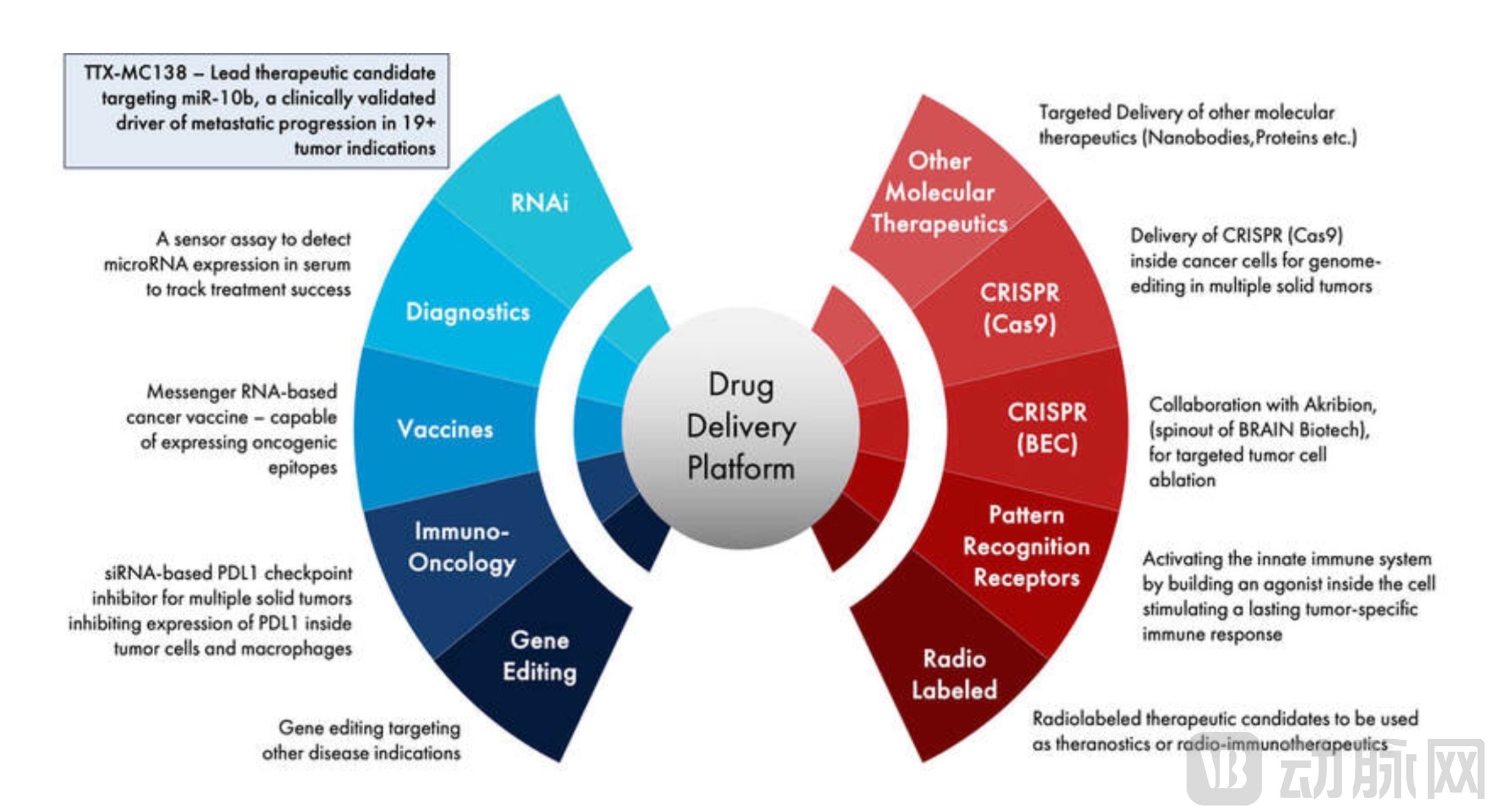
TransCode候选产品管道
图片来源:TransCode官网
此外,TransCode还部署了模块化工具箱来设计和开发广泛的候选产品管道。递送系统中的核心氧化铁纳米颗粒大小、电荷和表面化学工程都可以根据预期目标和治疗负荷进行调整优化。这一模块化工具箱可进一步开发RNA靶向放射标记治疗和生物标志物诊断等定制化产品。
除专有递送平台TTX系统外,TransCode另一大布局在于癌症药物的研发。主要治疗候选药物TTX-MC138靶向miRNA-10b,专注于治疗转移性癌症。转移指的是癌症从原发器官扩散到身体其他部位。转移性癌症是一个在传统药物研发上被忽视的领域。
根据2019年美国癌症协会报告,90%的癌症死亡是因为转移。传统临床治疗认为,非转移性与转移性肿瘤细胞的成分和治疗方式是相同的,疾病晚期患者只能改善预后,效果有限。
但基因检测与治疗领域的科学家发现,转移性癌症与原发肿瘤具有本质上的不同。这也为转移性癌症患者带来了新的治疗选择——基因靶向治疗。
miRNA-10b是最早在癌症中出现表达异常的miRNA之一。它在一系列癌症中担任肿瘤细胞活力和转移活力的主要调控因子,涉及部位包括乳腺、胰腺、卵巢、结肠、胶质母细胞瘤等。其高表达是转移性细胞的生存决定性要素。
具体而言,原发肿瘤中的部分细胞(即转移性细胞)会过度表达miRNA-10b。上调的miRNA-10b将允许转移性细胞从原发肿瘤细胞中分离,获得迁移和侵袭周围组织的能力,进而在体内形成新的肿瘤转移灶。
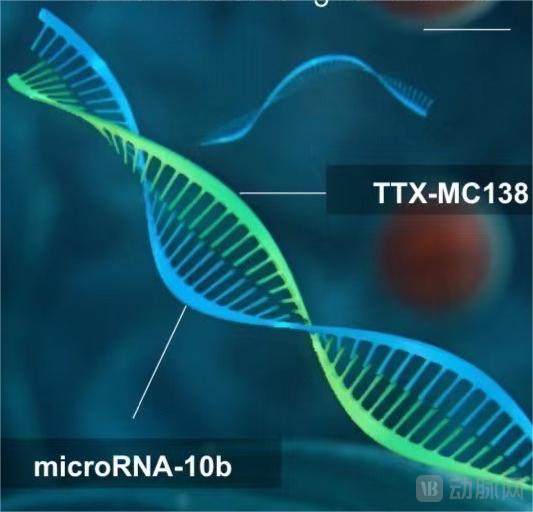
TTX-MC138与靶点miRNA-10b结合
图片来源:TransCode官网
TTX-MC138通过TTX系统递送至靶向组织后,将被转移性肿瘤细胞大量吸收,与miRNA-10b靶点结合。TTX-MC138将导致miRNA-10b的抑制和失活,进而实现肿瘤细胞死亡和疾病整体消退。在临床前实验中,成功实现递送的部位包括淋巴结、肺、骨、肝脏、肾脏、脾脏、肌肉。
此外,TTX-MC138独立于激素受体,因此不受激素受体类型影响,可应用于治疗转移性乳腺癌。这为治疗选择有限的三阴性乳腺癌(TNBC)患者提供了新的方案。在动物模型实验中,TTX-MC138药物与低剂量化疗配合治疗TNBC。
这一临床前实验证明,TTX-MC138在转移性乳腺癌小鼠模型中可持久消除已建立的转移灶。100%案例消除了局部转移(癌症转移至肺和淋巴结区域),65%案例消除了远处转移(癌症扩散至身体所有部位),且在停止治疗后没有发生转移或复发。
TTX-MC138还被应用于“癌症之王”胰腺癌的治疗之中。40%的单一治疗动物实现了完全反应,即疾病的100%消除且长期生存没有复发,miRNA-10b的表达下调了97%。针对这一适应症,TTX-MC138从FDA处获得了孤儿药指定(ODD)。
在胶质母细胞多形瘤中,TTX-MC138与替莫唑胺的组合治疗方案取得了积极的临床前结果,增强了替莫唑胺的细胞杀死能力,且成功抑制了肿瘤细胞的存活率和侵入性。
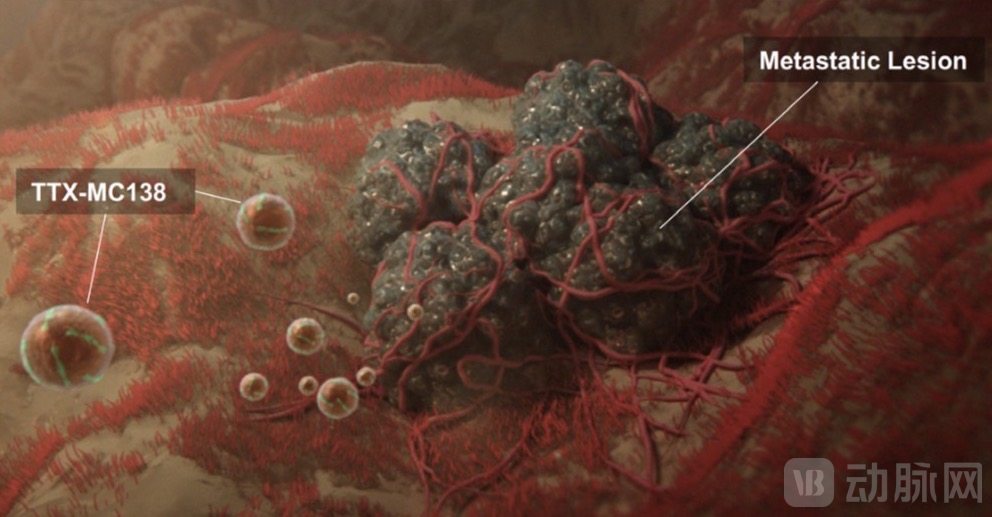
TTX-MC138模拟治疗过程
图片来源:TransCode官网
目前,FDA已授权TTX-MC138进行FIH 0期临床试验。这一试验将治疗12位患有晚期实体瘤的患者,评估TTX-MC138对其转移性病变的效果。FIH试验同时获得Dana Farber癌症研究所机构审查委员会(IRB)的书面批准。
专有递送平台为TransCode提供了深厚的研发基础和广阔的延申方向。目前,TransCode已开启TTX-CRISPR、TTX-RNA(癌症疫苗开发)两大治疗方案和四大癌症靶向药物的研发。
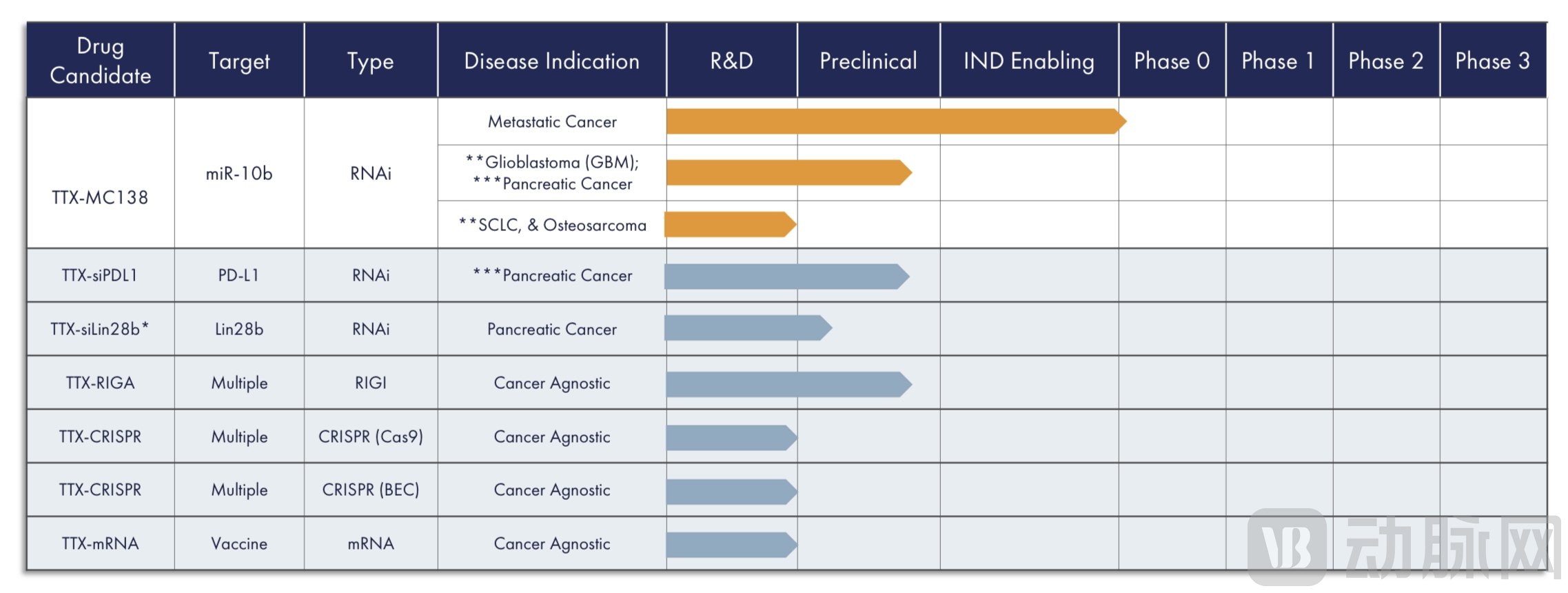
TransCode在研管线布局
图片来源:TransCode官网
除TTX-MC138外,TransCode有三款靶向药物处于临床前阶段。TTX-RIGA是一种治疗癌症的新型免疫候选药物,旨在与肿瘤细胞内的特异性RNA相结合,激活RIG-I(视甲酸诱导基因I)的细胞内受体,以驱动肿瘤微环境中的先天免疫反应。
TTX-siPDL1则是针对PD-1/PD-L1靶点的免疫治疗药物。相比传统抑制剂只是阻止二者组合,TTX-siPDL1采用RNAi方法完全阻止PD-L1的合成。因临床前动物实验的成功,TTX-siPDL1获得了FDA的胰腺癌孤儿药指定(ODD)。
TTX-siLin28B是靶向实体肿瘤的药物。Lin28B是一种肿瘤存活率的生物标志物。在此治疗方案中,TTX-siLin28B利用shRNA与siRNA降低Lin28B表达,从而有效抑制细胞增值和肿瘤块。此前,马萨诸塞州总医院(MGH)与TransCode签订TTX-siLin28b和64Cu-TTX-MC138的独家期权协议。
RNA领域的多方向延申也离不开创始团队多领域的医疗赛道背景。
联合创始人、首席执行官R.Michael Dudley曾创立Artemes Technologies。这是一家药物输送技术公司,专门从事注射药物的定制输送系统。这为其积攒了丰富的药物递送经验。此外,Michael Dudley早期曾在哈佛医学院进行乳腺癌肿瘤相关阻断因子的免疫学和生物化学研究,为其创办TransCode打下基础。
联合创始人、首席技术官Zdravka Medarova博士是一位遗传学家和癌症生物学家,以非编码RNA癌症治疗领域工作获得国际认可。她是最早应用纳米颗粒作为siRNA载体用于肿瘤治疗中的科学家之一。此前她一直在哈佛医学院担任放射学副教授,开发纳米技术和成像工具,应用于癌症诊断监测和抗癌治疗药物研发。
联合创始人Anna Moore博士现担任TransCode的科学顾问,曾任放射学和生理学教授、世界分子成像学会(WMIS)董事会前任成员。她在马赛诸纳州总医院Athinoula A. Martinos医学成像中心分子成像实验室担任主任长达18年。
三位联合创始人为TransCode提供了药物输送、癌症研究、纳米载体、分子成像等多领域学科背景。同时,TransCode也不断增强多领域学科的团队建设。
研发副总裁兼首席科学家Peter Liu博士拥有生物偶联化学、核酸化学和血液制品开发领域超过20年的研发和管理经验。另一位首席科学家Subarta Ghosh是一位免疫肿瘤学专家,主要研究方向为分子生物学、转化肿瘤学和创新联合疗法。他曾领导多项符合GLP的临床前研究、抗体和细胞研究设计和项目评估。
2016年,TransCode创建。
2021年,TransCode登陆纳斯达克,完成了总值2540万美元的IPO。
2023年,TransCode开始首次人体临床试验,公司进入临床研发阶段。
认股权证的发布是在出售未来,而TransCode的7年研发之路又何尝不是押注未来的赌约。
一家Therapeutics、一个创新靶点药、一种创新药,都是研发团队、医药公司与投资者的一场豪赌。有人被拍死在沙滩上,有人逆风翻盘,但创新医药的浪潮不止。
来源:动脉网 作者: 李秋萩