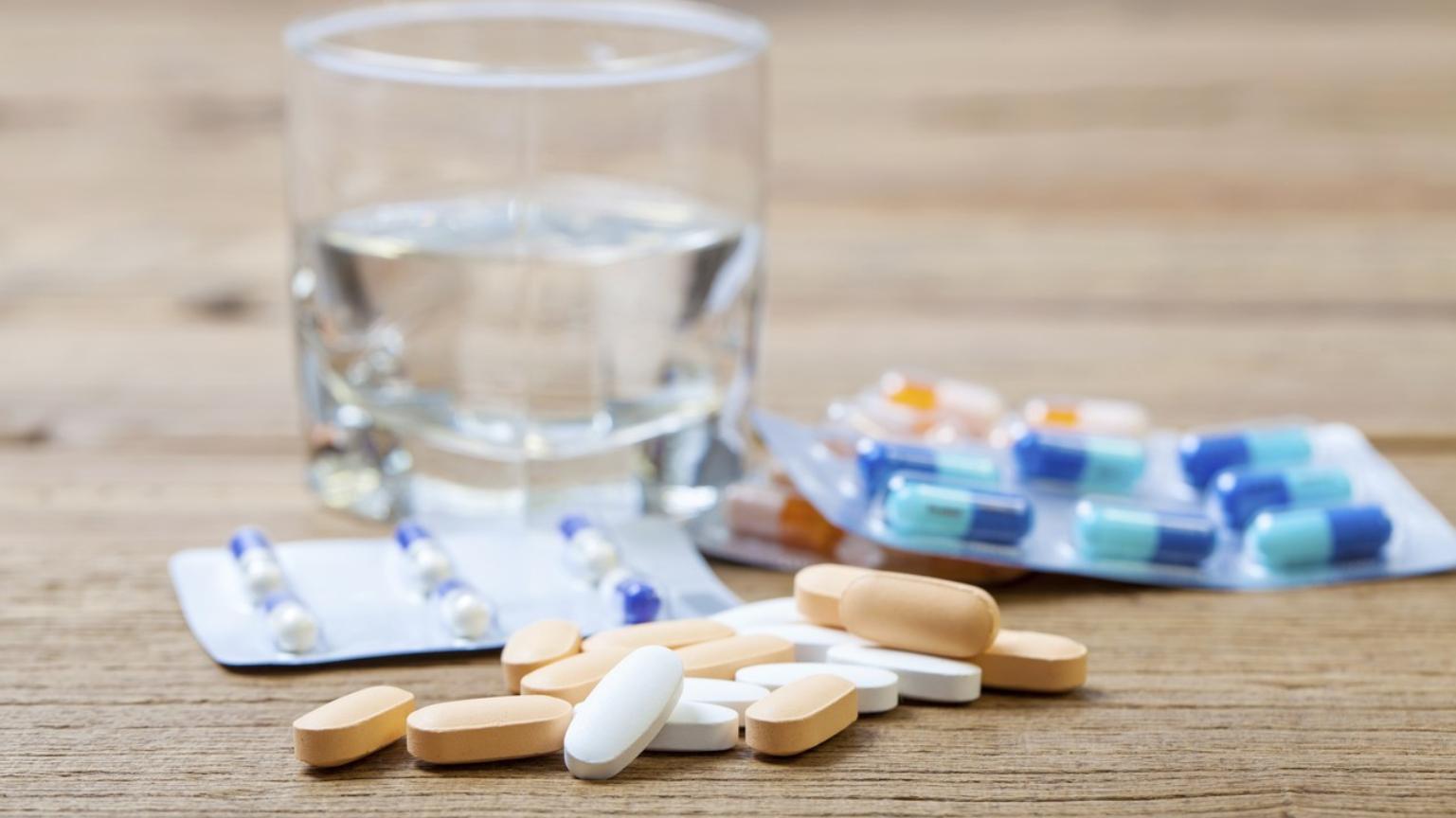
国家药品监督管理局药品审批中心官网显示,受理号分别为CXSS2200065和CXSS2200064的华东医药利拉鲁肽注射液的上市申请状态显示为暂停审批,作为华东医药在糖尿病领域的重磅产品,两个上市申请忽然被暂停,引发市场猜测。
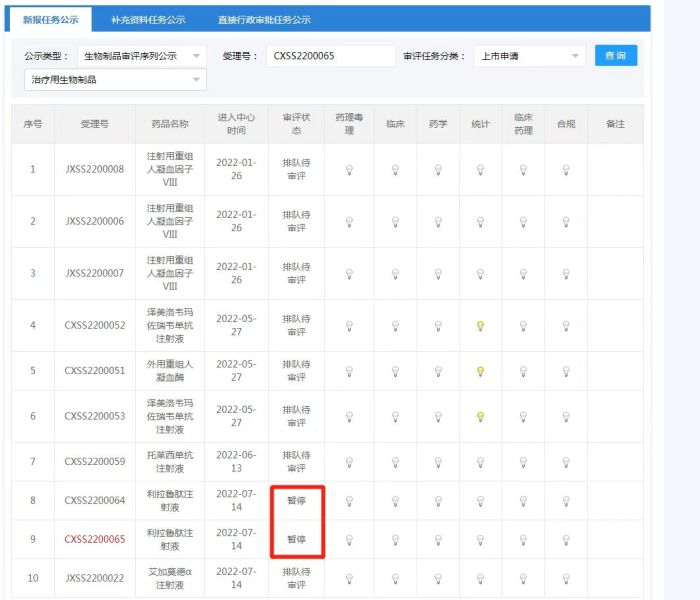
3月8日,华东医药方面对界面新闻记者回应称,这两个上市申报的是利拉鲁肽注射液的减肥适应症,因为年初疫情影响导致积压时间有所延长,需要提交一个剂量准确性的检验的补充要求报告,在此过程中处于暂停状态,否则审评会超出规定时间。
该上市申请“没有问题,不用担心”,华东医药方面称。
华东医药分别为利拉鲁肽注射液申请了两个适应症:其糖尿病适应症上市许可申请于2021年9月获国家药监局受理,目前处于发补研究阶段,预计有望于2022年底前获批上市;肥胖或超重适应症的上市许可申请于2022年7月获得受理。
2月22日,华东医药在答复投资者问答时表示,利拉鲁肽注射液糖尿病适应症及肥胖或超重适应症均有望在今年获批上市。
利拉鲁肽注射液是GLP-1受体激动剂。GLP-1受体广泛分布于全身多个器官和组织,包括胰腺、中枢神经系统、胃肠道、脂肪组织等。据《国际肥胖杂志》(International Journal of Obesity )的研究,肥胖患者餐时GLP-1分泌不足,因此GLP-1作用缺陷是肥胖的病生理学机制之一。此外,GLP-1作用于中枢上的GLP-1受体(特别是下丘脑)和中枢的饱涨中心,使人体产生饱胀感并降低食物的摄入,通过抑制食欲产生减肥的功效。这是利拉鲁肽注射液能被用于减肥的最核心逻辑。
而在国内,目前爱美人群对于使用GLP-1受体激动剂减肥更是追捧。诺和泰的中国收入达21.96亿丹麦克朗(约人民币20.85亿元),而这仅仅是其在中国的第一个完整销售年,该产品2021年4月才在国内获批上市。
因此,无论是在糖尿病还是减肥,利拉鲁肽都是市场高度关注的大品种。
2017年8月,华东医药子公司中美华东与杭州九源基因工程有限公司签订了《新药技术转让合同》,中美华东以8000万元受让对方拥有的利拉鲁肽新药技术。根据《新药技术转让合同》,中美华东成功受让利拉鲁肽新药技术并上市后的前6年里,每年需按其相关产品销售净额的3%提取并支付给杭州九源基因工程有限公司技术使用费。截至2022年6月30日,中美华东已累计支付新药技术转让款合计7200万元,利拉鲁肽新药技术尚未上市销售。
目前,诺和诺德原研的利拉鲁肽与司美格鲁肽都尚未在国内获批肥胖及超重适应症,但在糖尿病治疗领域,诺和诺德的利拉鲁肽注射液诺和力2017年首次被纳入国家医保目录并续约2021版国家医保目录、司美格鲁肽注射液诺和泰在国内上市不到4个月即被纳入国家医保目录报销体系。
在国内,已有多家上市企业入局利拉鲁肽生物类似药药。利拉鲁肽的化合物专利2017年已经到期、晶体专利2022年到期,国内华东医药、江苏万邦、爱美客的生物类似药均已处于临床阶段,其中华东医药进度最快,已经提交上市申请。
而另一款大热单品司美格鲁肽的序列结构专利和用途专利在中国于2026年3月到期,国内也已经有3家企业按生物类似药申报临床,去年6月以来,珠海联邦、九源基因、丽珠集团先后递交临床申报。华东医药司美格鲁肽注射液于2022年6月获得临床试验批准通知书。
围绕GLP-1类药物的单靶点、双靶点及多靶点研发亦竞争激烈。恒瑞医药此前在投资者互动平台表示,公司创新药诺利糖肽注射液用于治疗肥胖或超重合并至少一个体重相关并发症适应症目前处II期临床研发阶段;信达生物胰高血糖素样肽-1受体/胰高血糖素受体双重激动剂Mazdutide (IBI362)在中国二型糖尿病受试者中的II期临床研究中达到主要终点。
来源:界面新闻
作者:李科文